La Noche que Nació la PCR: Una Epifanía Científica en la Carretera
La Noche que Nació la PCR: Una Epifanía Científica en la Carretera
¡Hola a todos los amantes de la ciencia! Hoy nos sumergimos en un relato fascinante de descubrimiento, contado en primera persona por el mismísimo Kary Mullis, premio Nobel y el genio detrás de la Reacción en Cadena de la Polimerasa (PCR).
Acompáñenme en este viaje nocturno que cambiaría la bioquímica para siempre, una historia de intuición, desafíos y el destello de genialidad que transformó una rama de la ciencia. Prepárense para conocer la mente de un pionero mientras desentrañamos los momentos clave que llevaron a la creación de una de las herramientas más poderosas en la biología molecular moderna.
Una Noche en la Carretera: El Destello de una Idea
Una noche de viernes, mi costumbre era conducir desde Berkeley hasta Mendocino, donde tengo una cabaña en medio del bosque, lejos de todo. Mi novia, Jennifer Barnett, dormía plácidamente. Yo, sin embargo, estaba inmerso en mis pensamientos. Con los oligonucleótidos, esas pequeñas cadenas de ADN, ya no tan difíciles de sintetizar, me pregunté: ¿no sería lo suficientemente simple poner dos de ellos en la reacción en lugar de solo uno?
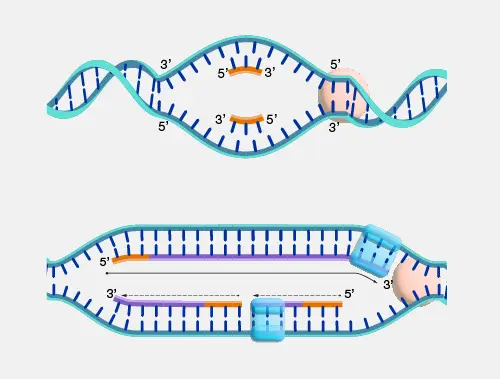
La idea era que uno se uniera a la hebra superior y el otro a la hebra inferior, con sus extremos tres prima adyacentes a las bases opuestas del par de bases en cuestión. Si uno se hacía más largo que el otro, entonces sus productos de extensión de una sola base podrían separarse en un gel, y uno podría actuar como control del otro. De todos modos, tendría que separarlos en un gel del gran exceso de nucleósidos trifosfatos radiactivos. Lo que esperaría ver es que uno de ellos recogiera un nucleótido radiactivo y el otro recogiera su complemento. Otras combinaciones indicarían que algo había salido mal. No era un control perfecto, pero no requeriría mucho esfuerzo. Estaba a punto de llevarme a la PCR.
La Elegancia del Control y el Aroma de la Noche
Me encantó la idea de un control que fuera casi gratuito en términos de costo y esfuerzo. Además, ayudaría a consumir los oligonucleótidos que mi laboratorio ahora podía fabricar más rápido de lo que se podían usar.
Mientras conducía por las montañas esa noche, los tallos de los castaños de indias de California, en plena floración, se inclinaban hacia la carretera. El aire era húmedo y fresco y estaba lleno de su embriagador aroma.
Desafíos Bioquímicos y la Fosfatasa Alcalina Bacteriana
Animado por mi progreso en el experimento mental, seguí pensando en ello y en las cosas que podrían salir mal. ¿Qué pasaría si hubiera desoxinucleósidos trifosfatos en la muestra de ADN, por ejemplo? Lo que pasaría, razoné, es que uno o más de ellos se añadirían al oligonucleótido por la polimerasa antes de la terminación de la elongación de la cadena por adición del didesoxinucleósido trifosfato. Esto podría llevar a un producto de extensión de tamaño incorrecto y resultados erróneos. ¡No serviría!
Necesitaba una forma de asegurar que la muestra estuviera libre de contaminación por desoxinucleósidos trifosfatos. Podría tratar la muestra antes de la reacción de extensión con fosfatasa alcalina bacteriana (BAP). Esta enzima degradaría cualquier trifosfato presente a nucleósidos que no interferirían con la reacción principal. Pero entonces necesitaría «desactivar» la fosfatasa antes de añadir los didesoxinucleósidos trifosfatos.
En ese momento, todos sabían que la BAP no era irreversiblemente desnaturalizable por el calor. La razón era que la renaturalización de la BAP desnaturalizada por calor se había demostrado en experimentos clásicos, mostrando que la forma de una proteína está dictada por su secuencia. En esos experimentos, la renaturalización se había realizado en un tampón con mucho zinc.
Lo que no se me había ocurrido a mí, ni aparentemente a muchos otros, era que la BAP podría desnaturalizarse irreversiblemente si se omitía el zinc del tampón, y que el zinc no era necesario si la enzima solo se iba a usar por un corto tiempo y tenía su propio zinc fuertemente unido desde el principio.
Existía un producto en el mercado llamado matBAP, donde la enzima estaba unida a una matriz insoluble que podía filtrarse de una solución después de su uso. El producto se vendía porque la gente tenía la impresión de que no se podía desnaturalizar la BAP irreversiblemente. Todos habíamos oído hablar, pero no leído, de los artículos clásicos.
El Giro Inesperado que Llevó a la PCR
Esto dice algo sobre la forma arbitraria en que se establecen muchos hechos científicos, pero para esta historia, su única importancia es que, si hubiera sabido entonces que la BAP podía desnaturalizarse por calor irreversiblemente, podría haberme perdido la PCR. Tal como estaba, decidí no usar BAP y traté de pensar en otra forma de deshacerme de los desoxinucleósidos trifosfatos. ¿Qué tal esto, pensé? ¿Qué pasaría si omito los didesoxinucleósidos trifosfatos radiactivos, mezclo la muestra de ADN con los oligonucleótidos, añado la polimerasa y espero?
La polimerasa debería consumir todos los desoxinucleósidos trifosfatos añadiéndolos a los oligonucleótidos hibridados. Una vez completado esto, podría calentar la mezcla, haciendo que los oligonucleótidos extendidos se separaran del objetivo, luego enfriar la mezcla permitiendo que se hibridaran oligonucleótidos nuevos y no extendidos. Los oligonucleótidos extendidos serían superados en número por el vasto exceso de oligonucleótidos no extendidos y, por lo tanto, no se re-hibridarían al objetivo en gran medida. Luego añadiría las mezclas de didesoxinucleósidos trifosfatos y otra alícuota de polimerasa. ¡Y ahora las cosas funcionarían!
¡EUREKA! Nace la Reacción en Cadena de la Polimerasa
Pero, ¿qué pasaría si los oligonucleótidos en la reacción de extensión original se hubieran extendido tanto que ahora pudieran hibridarse con oligonucleótidos no extendidos de polaridad opuesta en esta segunda ronda? La secuencia en la que se habían extendido lo permitiría. ¿Qué pasaría?
¡¡¡EUREKA!!!! El resultado sería exactamente el mismo, solo que la fuerza de la señal se duplicaría.

¡¡¡EUREKA de nuevo!!!! Podría hacerlo intencionalmente, añadiendo mis propios desoxinucleósidos trifosfatos, que eran bastante solubles en agua y legales en California.
Y de nuevo, ¡¡¡EUREKA!!!! Podría hacerlo una y otra vez. Cada vez que lo hiciera, duplicaría la señal. Para los que se perdieron, ¡hemos vuelto! Detuve el coche en el marcador de milla 46,7 de la Autopista 128. En la guantera encontré papel y un bolígrafo. Confirmé que dos elevado a la décima potencia era aproximadamente mil, que dos elevado a la vigésima potencia era aproximadamente un millón, y que dos elevado a la trigésima potencia era alrededor de mil millones, cerca del número de pares de bases en el genoma humano. Una vez que hubiera ciclado esta reacción treinta veces, podría obtener la secuencia de una muestra con una señal inmensa y casi sin ruido de fondo.
Un Destello que Cambió la Química del ADN
Jennifer quería seguir adelante. Conduje por la carretera. En aproximadamente una milla se me ocurrió que los oligonucleótidos podrían colocarse a una distancia arbitraria entre sí, no solo flanqueando un par de bases, y que podría hacer un número arbitrariamente grande de copias de cualquier secuencia que eligiera y, lo que es más, la mayoría de las copias después de unos pocos ciclos tendrían el mismo tamaño. Ese tamaño dependería de mí. Se parecerían a fragmentos de restricción en un gel. Detuve el coche de nuevo.
«¡Querido Thor!», exclamé. Había resuelto los problemas más molestos de la química del ADN en un solo relámpago: Abundancia y distinción. Con dos oligonucleótidos, ADN polimerasa y los cuatro nucleósidos trifosfatos, podía hacer tanto de una secuencia de ADN como quisiera y podía hacerlo en un fragmento de un tamaño específico que podía distinguir fácilmente.
De alguna manera, pensé, tenía que ser una ilusión. De lo contrario, cambiaría la química del ADN para siempre. De lo contrario, me haría famoso. Era demasiado fácil. Alguien más lo habría hecho y seguramente habría oído hablar de ello. Lo estaríamos haciendo todo el tiempo. ¿Qué no estaba viendo? «Jennifer, despierta. He pensado en algo increíble.»
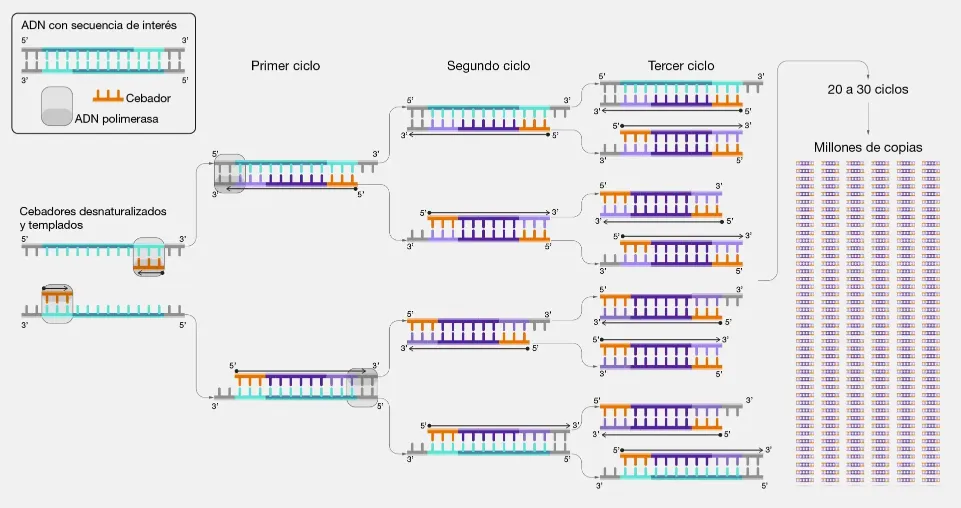
La Incredulidad y el Amanecer de una Nueva Era
Ella no se despertaba. Ya había pensado en cosas increíbles que de alguna manera perdían parte de su brillo a la luz del día. Esta podía esperar hasta la mañana. Pero no dormí esa noche. Llegamos a mi cabaña y empecé a dibujar pequeños diagramas en cada superficie horizontal que aceptara pluma, lápiz o crayón hasta el amanecer, cuando, con la ayuda de una última botella de buen cabernet del condado de Mendocino, me sumí en una semiinconsciencia perpleja.
Llegó la tarde, incluyendo nuevas botellas de fluidos rojos de celebración de Jack’s Valley Store, pero yo seguía perplejo, alternando entre estar absolutamente complacido con mi buena suerte y mi cerebro inteligente, y estar ligeramente molesto conmigo mismo y con Jennifer Barnett, por no ver el defecto que debía haber estado allí. No tenía teléfono en la cabaña y no había otros bioquímicos además de Jennifer y yo en Anderson Valley.
El enigma que persistió durante todo el fin de semana y creó en mí un deseo sin precedentes de volver a trabajar temprano era convincente. Si las reacciones cíclicas que para entonces estaban simbolizadas de varias maneras por toda la cabaña realmente funcionaban, ¿por qué nunca había oído hablar de su uso? Si se hubieran usado, seguramente habría oído hablar de ello y también todos los demás, incluida Jennifer, que en ese momento tomaba el sol junto al estanque sin interesarse por las explosiones que sacudían mi cerebro.
¡Y así nació la PCR, una herramienta que revolucionaría la biología molecular! Permanezcan atentos para más historias de descubrimientos científicos que cambiaron nuestro mundo.
Referencias
Fragmento de la conferencia Nobel de Kary B. Mullis (1993), “The Polymerase Chain Reaction”. Texto completo en: Kary B. Mullis – Nobel Lecture. NobelPrize.org. Nobel Prize Outreach 2025. Tue. 16 Dec 2025. <https://www.nobelprize.org/prizes/chemistry/1993/mullis/lecture/>






