Medicina de precisión: CRISPR logra su primera cura personalizada
La era de la medicina personalizada ha comenzado
Estamos ante un cambio paradigmático en la medicina gracias a la edición genética. El caso de KJ, un bebé diagnosticado con una enfermedad metabólica llamada deficiencia de carbamil fosfato sintetasa 1 (CPS1), es un hito en la medicina personaliza y un ejemplo excepcional que muestra cómo la tecnología CRISPR puede transformar la vida de pacientes con enfermedades genéticas que antes se consideraban incurables.

¿Qué es la deficiencia de CPS1 y por qué es tan grave?
La deficiencia de CPS1 es una enfermedad genética causada por mutaciones en el gen CPS1, que codifica para una enzima fundamental en el ciclo de la urea, un proceso metabólico clave para eliminar el amonio tóxico que se produce al digerir proteínas. El amonio es un subproducto del metabolismo de los aminoácidos, y su acumulación en sangre es extremadamente dañina, especialmente para el cerebro, pudiendo causar daño neurológico severo o la muerte si no se elimina eficazmente.
En condiciones normales, la enzima CPS1 convierte el amonio en carbamil fosfato, iniciando una serie de reacciones que finalmente eliminan el amonio en forma de urea a través de la orina. Pero en KJ, por la presencia de mutaciones en ambas copias del gen (una heredada de cada progenitor), esta enzima no se produce o funciona mal. Esto provoca una intoxicación progresiva que afecta gravemente su desarrollo y pone en riesgo su vida desde los primeros días.
¿Cómo funciona la edición genética CRISPR en este contexto?
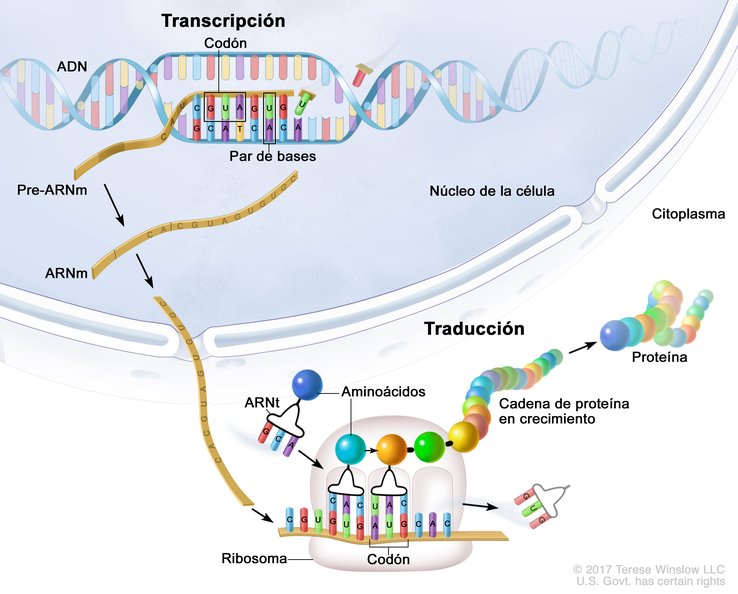
La técnica utilizada para tratar a KJ es una evolución de la tecnología CRISPR-Cas9, conocida como “tijeras genéticas”. Sin embargo, en este caso se aplicó una variante llamada edición de bases (base editing), que funciona como un corrector ortográfico molecular: puede cambiar una única letra del ADN —una base nitrogenada— sin cortar completamente la cadena genética.
Esta precisión permite corregir la mutación puntual específica que causa la deficiencia de CPS1 en KJ, restaurando la función del gen sin introducir roturas que podrían generar efectos secundarios indeseados.
El proceso del tratamiento: del laboratorio al paciente
- Identificación y diseño del editor genético: se secuenció el ADN de KJ para identificar la mutación específica y se diseñó un editor de bases para corregir la mutación heredada del padre.
- Pruebas en células propias de KJ: se extrajeron células del bebé para probar distintas versiones del editor en el laboratorio y elegir la más eficaz y segura.
- Entrega del editor genético: se usaron nanopartículas lipídicas, similares a las usadas en vacunas ARNm, para transportar el editor genético al hígado.
- Validación en modelos animales: se probaron en ratones humanizados y primates no humanos antes de su aplicación en KJ.
- Aplicación en KJ: tras tres dosis administradas durante varios meses, los niveles de amonio en sangre se normalizaron y el bebé pudo comenzar a alimentarse y salir del hospital.
¿Por qué es tan importante este caso para la medicina personalizada?
Este tratamiento representa la esencia de la medicina personalizada: una terapia adaptada genéticamente al defecto específico de un solo paciente. Es un tratamiento único, diseñado a medida, que actúa directamente sobre el ADN defectuoso.
Lo extraordinario es que esta terapia fue desarrollada y aplicada en menos de seis meses, superando rigurosas pruebas de seguridad y eficacia. KJ mostró una notable mejoría: normalización del amonio, mayor tolerancia a proteínas y, por primera vez, pudo salir del hospital.
Aspectos por resolver
Este avance, publicado en el New England Journal of Medicine, demuestra el potencial transformador de la edición genética. Sin embargo, persisten dudas importantes:
- ¿Será duradera la corrección en el hígado?
- ¿Habrá que repetir la terapia?
- ¿Será inevitable un trasplante en el futuro?
Además, el alto costo y la complejidad técnica hacen que este tipo de tratamiento aún no sea accesible para todos. Pero la historia nos muestra que la innovación tecnológica suele abaratarse con el tiempo. Hoy, secuenciar un genoma cuesta menos de 1,000 dólares, cuando hace dos décadas costaba más de 2,700 millones. Esto nos da motivos reales para el optimismo.
Conclusión
El caso de KJ es un hito en la historia de la medicina. Gracias a CRISPR, se corrigió una mutación genética específica, logrando lo que hasta hace poco parecía imposible: curar una enfermedad metabólica ultra rara mediante una intervención genética precisa.
Este éxito abre la puerta a una nueva era en la que los tratamientos estarán diseñados genéticamente para cada individuo, dejando atrás el modelo de “talla única” que ha dominado la medicina durante décadas. Aunque todavía quedan retos importantes por resolver, la medicina personalizada, potenciada por herramientas como CRISPR, se perfila como el futuro de la salud.
Estamos presenciando una verdadera revolución científica que cambiará para siempre la forma en que entendemos, tratamos y —sobre todo— curamos las enfermedades humanas.
Referencias:
- Musunuru, K., Grandinette, S. A., Wang, X., Hudson, T. R., Briseno, K., Berry, A. M., … & Ahrens-Nicklas, R. C. (2025). Patient-specific in vivo gene editing to treat a rare genetic disease. New England Journal of Medicine, 392(22), 2235-2243. DOI: 10.1056/NEJMoa2504747.
- The Children’s Hospital of Philadelphia. (2025, mayo 12). World’s first patient treated with personalized CRISPR gene editing therapy at children’s hospital of Philadelphia. Chop.edu. https://www.chop.edu/news/worlds-first-patient-treated-personalized-crispr-gene-editing-therapy-childrens-hospital